Гост 14921-78 газы углеводородные сжиженные. методы отбора проб (с изменениями n 1, 2, 3)
Содержание:
- Промышленное производство
- Клиническая информация, средства защиты, первоочередные действия в очаге
- ОПРЕДЕЛЕНИЕ ОБЪЕМНОЙ ДОЛИ ВОДЯНОГО ПАРА КОНДЕНСАЦИОННЫМ МЕТОДОМ
- Хранение и соблюдение техники безопасности
- В чем хранится и транспортируется технический азот
- Диоксид азота класс опасности
- Безопасность
- ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
- Немного истории открытия азота
- Конструктивные особенности изотермической цистерны для транспортировки жидкого азота:
- Физические характеристики вещества
- Токсичность и опасность
- Автомобильная транспортировка азота
- Диоксид азота
Промышленное производство
В настоящее время в основном используют три технологии для получения инертного азота, основанные на разделении атмосферного воздуха:
- криогенная;
- мембранная;
- адсорбционная.
Разделяющие криогенные установки функционируют по принципу сжижения воздуха. Сначала он сжимается компрессором, затем проходит через теплообменники и расширяется в детандере. В результате охлажденный воздух становится жидкостью. За счет разной температуры кипения кислорода и азота происходит их разделение. Процесс многократно повторяется на специальных ректификационных тарелках. Завершается он получением чистейшего кислорода, аргона и азота. Данный способ наиболее эффективен для крупных предприятий по причине значительных габаритов системы, сложности ее пуска и обслуживания. Достоинство метода состоит в том, что можно получить азот наивысшей чистоты, как жидкий, так и газообразный, в любых количествах. При этом расход энергии на изготовление 1 л вещества составляет 0,4-1,6 кВт/ч (в зависимости от технологической схемы установки).
Мембранная технология разделения газов начала применяться в 70-х годах прошлого века. Высокая экономичность и эффективность данного метода послужила достойной альтернативой криогенному и адсорбционному способам получения чистого азота. Сегодня в установках используются мембраны последнего поколения высокой производительности. Теперь это не пленка, а тысячи полых волокон, на которые нанесен селективный слой. Подвижные составляющие в установке отсутствуют, поэтому значительно увеличивается продолжительность ее эксплуатации без поломок. Отфильтрованный воздух подается в систему. Кислород беспрепятственно проходит сквозь нее, а азот выводится под давлением через противоположную сторону мембраны и направляется в накопитель. С помощью данных установок изготавливается вещество с чистотой до 99,95%. Таким образом осуществляется производство азота из атмосферного воздуха. Ограниченная чистота получаемого азота не позволяет применять данный метод крупным изготовителям с большими потребностями высокочистого азота.
На тех предприятиях, где востребован азот высокой чистоты в больших объемах, применяется установка для разделения газовых смесей при помощи адсорбентов. Конструктивно она представляет собой две колонны. В каждой из них находится вещество, селективно поглощающее газовую смесь. Для функционирования установок по производству азота требуется атмосферный воздух, электроэнергия.
Изначально воздух попадает в компрессор, где происходит его сжатие. Затем он подается в ресивер, который выравнивает его давление. Так как воздух не должен содержать водяных паров, пыли, двуокиси углерода, окислов азота, ацетилена, а также других примесей, его фильтруют. Наступает основной этап адсорбционного разделения газовой смеси. Поток воздуха пропускается через одну колонну с углеродными молекулярными ситами до тех пор, пока они способны поглощать кислород. После этого поверхность адсорбента необходимо очистить, то есть регенерировать, путем сброса давления или повышением температуры. А воздух направляется во вторую колонну. В это время азот проходит сквозь агрегат и накапливается в ресивере. Продолжительность циклов адсорбции и регенерации составляет всего несколько минут. Чистота получаемого по данной технологии азота составляет 99,9995%.
Преимущества адсорбционных установок:
- быстрый пуск и остановка;
- возможность дистанционного управления;
- высокая разделительная способность;
- низкое энергопотребление;
- возможность оперативной переналадки;
- автоматическое регулирование режима;
- низкие затраты на обслуживание.
Клиническая информация, средства защиты, первоочередные действия в очаге
| Общий характер действия |
|
Средства защиты
Для химразведок и руководителя работ — ПДУ-3 (в течение 20 минут). Для аварийных бригад — изолирующий противогаз ИП-4М и спецодежда.
Химический очаг
Вид очага
Стойкий, замедленного действия очаг. Пары тяжелее воздуха, могут скапливаться в низинах, подвалах. тоннелях.
Первоочередные мероприятия
Проведение поисково-спасательных работ в очаге, в том числе оказание первой медицинской помощи пострадавшим и их вынос (вывоз) на временные пункты сбора в оптимальные для спасения жизни и сохранения здоровья сроки, ведение разведки, обозначение и оцепление очага. Изолировать опасную зону в радиусе не менее 200 м. Откорректировать указанное расстояние по результатам химразведки. Держаться наветренной стороны. Избегать низких мест. В опасную зону входить в защитных средствах
Устранить течь с соблюдением мер предосторожности. При интенсивной утечке дать газу полностью выйти
Не допускать контакта с ма слами (нефтепродуктами), горючими веществами. Изолировать район, пока газ не рассеется. Не приближаться к емкостям. Охлаждать емкости водой с максимального расстояния. В случае возгорания в окрестностях разрешены все средства пожаротушения.
ОПРЕДЕЛЕНИЕ ОБЪЕМНОЙ ДОЛИ ВОДЯНОГО ПАРА КОНДЕНСАЦИОННЫМ МЕТОДОМ
1. Объемную долю водяного пара определяют приборами конденсационного типа с пороговой чувствительностью не выше 1,5 млн-1.
Относительная погрешность прибора не должна превышать 10 %.
Метод основан на измерении температуры насыщения газа водяным паром при появлении росы на охлажденной зеркальной поверхности.
Анализ проводят по инструкции, приложенной к прибору.
Объемную долю водяного пара в соответствии с найденной температурой насыщения определяют по таблице.
|
Объемная доля водяного пара, млн-1 (ppm) |
Температура насыщения, C |
Объемная доля водяного пара, млн-1 (ppm) |
Температура насыщения, C |
|
2,55 |
-70 |
23,4 |
-54 |
|
3,44 |
-68 |
31,1 |
-52 |
|
4,60 |
-66 |
39,4 |
-50 |
|
6,10 |
-64 |
49,7 |
-48 |
|
8,07 |
-62 |
63,2 |
-46 |
|
10,6 |
-60 |
80 |
-44 |
|
14,0 |
-58 |
101 |
-42 |
|
18,3 |
-56 |
127 |
-40 |
Примечание. Объемная доля, равная 1 млн-1, соответствует 1. 10-4 %.
(Измененная редакция, Изм. № 3).
ПРИЛОЖЕНИЕ 2Рекомендуемое
1. Объем газообразного азота в стальном баллоне (Vп) в м3 при 20°С и 101,3 кПа вычисляют по формуле
Vп=K . Vб,
где Vб— вместимость баллона, дм3. В расчетах принимается среднестатистическая величина вместимости баллонов не менее чем из 100 шт.;
К — коэффициент для вычисления объема газа в баллоне, учитывающий сжимаемость азота, давление и температуру газа в баллоне, вычисляют по формуле
,
где Р — давление газа в баллоне, измеренное манометром, кгс/см2;
0,968 — коэффициент пересчета технических атмосфер (кгс/см2) в физические атмосферы;
t — температура газа в баллоне при измерении давления, °С;
Z — коэффициент сжимаемости азота при температуре t°С, указанный в таблице.
|
Давление, МПа, (кгс/см2) |
Температура, °С |
|||||
|
-50 |
-25 |
20 |
25 |
50 |
||
|
Коэффициент сжимаемости азота |
||||||
|
10(100) |
0,905 |
0,918 |
0,985 |
1,001 |
1,005 |
1,018 |
|
14,5(145) |
0,93 |
0,95 |
1,001 |
1,02 |
1,023 |
1,037 |
|
20,4 (200) |
0,958 |
0,968 |
1,035 |
1,053 |
1,06 |
1,076 |
Например, при поставке газообразного азота в баллонах по ГОСТ 949-73 вместимостью 40 дм3 количество газа в баллоне при рабочем давлении 150 кгс/см2 при 20°С составляет
.
2. Количество жидкого азота, отпускаемого потребителю в транспортных цистернах, определяют по указателю уровня жидкого азота (УЖА) в тоннах.
При переводе массы жидкого азота в м3 газообразного азота при 20°С и 101,3 кПа пользуются формулой
,
где т — масса жидкого азота, т;
1,165 — плотность газообразного азота, кг/м3.
Приложение 3 — исключено.
(Измененная редакция, Изм. № 3).
|
4. Упаковка, маркировка, транспортирование и хранение Определение объемной доли водяного пара конденсационным методомОпределение количества азота, отпускаемого потребителю |
Хранение и соблюдение техники безопасности
Автотранспортом азот в жидком состоянии перевозят в специальных криогенных сосудах или цистернах. Потребителям доставляют газообразное вещество в сжатом виде в черных баллонах. Хранят азот в сосудах Дьюара, имеющих двойные стенки, между которыми находится вакуум. В целях уменьшения передачи тепла поверхности делают зеркальными за счет слоя серебра. Сосуды Дьюара могут быть разного объема. Емкости, вмещающие десятки литров, изготавливают из металла. В таком сосуде вещество может храниться несколько недель.
Кратковременный контакт кожи с жидким азотом не представляет серьезной опасности, так как в месте соприкосновения образуется воздушная подушка, обладающая низкой теплопроводностью. Именно она защищает ткани от травмирования. Длительный контакт азота с кожей, глазами или слизистыми оболочками вызывает их тяжелое повреждение. Пораженный участок при попадании вещества необходимо незамедлительно промыть большим количеством воды.
При испарении азота происходит его накопление на уровне пола рабочего помещения из-за низкой температуры и большей плотности, чем у воздуха. Незаметно для человека создается высокая концентрация вещества, а количество кислорода уменьшается. Это влияет на общее самочувствие: нарушается ритм дыхания и учащается пульс. При тяжелом исходе ситуации расстраивается сознание и теряется способность двигаться. Опасность состоит в том, что отравление происходит незаметно для человека, пострадавший не осознает серьезности ситуации. Поэтому помещения, в которых производится или используется азот, обязательно оснащаются надежной системой вентиляции.
В чем хранится и транспортируется технический азот
Хранение и перевозка газообразного вещества осуществляется в баллонах из стали (ГОСТ 949-73) черного цвета с желтой надписью. Сжиженный газ транспортируется в специальных цистернах или криогенных резервуарах.

На рисунке показаны баллоны для хранения и транспортировки технического азота
До недавнего времени эксплуатация жидкого азота как инертного вещества считалась абсолютно безопасной. Однако, на сегодня известно несколько случаев взрывов резервуаров и оборудования, работающего со сжиженным N2, что вызвано быстрым испарением жидкой фазы и обогащением ее кислородом. Поэтому при эксплуатации житкоазотных сосудов необходимо руководствоваться такими же требованиями, как и при работе с резервуарами с жидким кислородом.
Во время перевозки газообразного состава необходимо избегать ударов и падений сосудов, а также их перегрева. Поскольку внутреннее давление емкости составляет 15-20 Мпа, при сильном ударе или нагреве более 60°C появляется риск разгерметизации или взрыва.
Азотный баллон, как и любая емкость, работающая под давлением, должен периодически подвергаться переаттестации. При этом к качеству и чистоте резервуара предъявляются, как правило, более высокие требования, чем, например, к сосудам, предназначенным для заправки CO2. Кстати, интересную информацию о свойствах и процессе заправки углекислоты можно прочитать в статье: углекислота: где заправить – вопрос не праздный.

Специалист осматривает баллон для его переаттестации
Степень опасности для человека
Несмотря на то, что N2 является нетоксичным и не имеет отрицательного влияния на окружающую среду, для человека его действие может иметь весьма неприятные последствия. Замещая в атмосфере и вытесняя из организма кислород, данный газ работает как удушающий агент. При уменьшении концентрации кислорода в воздухе ниже 19% человек начинает испытывать следующие симптомы:
- учащение дыхания и пульса;
- головокружение;
- чувство тяжести и жара в теле;
- затруднение речи;
- снижение работоспособности;
- возможная потеря сознания.
Поэтому при работе в азотной среде важно придерживаться основных мер безопасности – часто проветривать помещение и контролировать содержание O2
Диоксид азота класс опасности
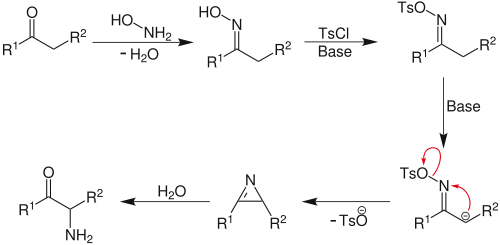
В лаборатории NO2 обычно получают воздействием концентрированной азотной кислотой на медь:
Также его можно получить термическим разложением нитрата свинца, однако при проведении реакции следует соблюдать осторожность:
Химические свойства
Кислотный оксид, ему соответствуют азотная и азотистая кислоты. NO2 отличается высокой химической активностью. Он взаимодействует с неметаллами (фосфор, сера и углерод горят в нём). В этих реакциях NO2 — окислитель:
Окисляет SO2 в SO3 — на этой реакции основан нитрозный метод получения серной кислоты:
При растворении оксида азота(IV) в воде образуются азотная и азотистая кислоты (реакция диспропорционирования):
Поскольку азотистая кислота неустойчива, при растворении NO2 в тёплой воде образуются HNO3 и NO:
Если растворение проводить в избытке кислорода, образуется только азотная кислота (NO2 проявляет свойства восстановителя):
При растворении NO2 в щелочах образуются как нитраты, так и нитриты:
Применение
В производстве серной и азотной кислот, в качестве окислителя в жидком ракетном топливе и смесевых взрывчатых веществах.
Физиологическое действие
Оксид азота (IV) высоко токсичен. Даже в небольших концентрациях он раздражает дыхательные пути, в больших концентрациях вызывает отёк лёгких.
«Лисий хвост»
«Лисий хвост» — жаргонное название выбросов в атмосферу оксидов азота на химических предприятиях (иногда – из выхлопных труб “плохих” автомобилей).
Название
Название происходит от оранжево-бурого цвета диоксида азота. При низких температурах диоксид азота димеризуется и становится бесцветным. В летний сезон «лисие хвосты» наиболее заметны, так как в выбросах возрастает концентрация мономерной формы.
Вредное воздействие
Оксиды азота, улетучивающиеся в атмосферу, представляют серьезную опасность для экологической ситуации, так как способны вызывать кислотные дожди, а также сами по себе являются токсичными веществами, вызывающими раздражение слизистых оболочек.
Диоксид азота воздействует в основном на дыхательные пути и легкие, а также вызывает изменения состава крови, в частности, уменьшает содержание в крови гемоглобина.
В специальной литературе также указывается на то, что воздействие на организм человека диоксида азота снижает сопротивляемость к заболеваниям, вызывает кислородное голодание тканей, особенно у детей. Усиливает действие канцерогенных веществ, способствуя возникновению злокачественных новообразований.
Образующаяся в результате взаимодействия диоксида азота с водой азотная кислота является сильным коррозионным агентом.
Wikimedia Foundation . 2010 .
Смотреть что такое “Диоксид азота” в других словарях:
диоксид азота — — [http://www.eionet.europa.eu/gemet/alphabetic?langcode=en] EN nitrogen diox >Справочник технического переводчика
диоксид азота (NO2) — 3.5.4 диоксид азота (NO2): Продукт, относящийся к классу опасности 2 по title= Предельно допустимые концентрации (ПДК) загрязняющих веществ в атмосферном воздухе населенных мест . Источник … Словарь-справочник терминов нормативно-технической документации
азота диоксид — azoto(IV) oks >Chemijos terminų aiškinamasis žodynas
азота двуокись — azoto(IV) oks >Chemijos terminų aiškinamasis žodynas
азота(IV) оксид — azoto(IV) oks >Chemijos terminų aiškinamasis žodynas
АЗОТА ОКСИДЫ — АЗОТА ОКСИДЫ: гемиоксид N2O и монооксид NO (бесцветные газы) сесквиоксид N2O3 (синяя жидкость), диоксид NO2 (бурый газ, при обычных условиях смесь NO2 и его димера N2O4), оксид N2O5 (бесцветные кристаллы). N2O и NO несолеобразующие оксиды, N2O3 с … Большой Энциклопедический словарь
АЗОТА ОКСИДЫ — АЗОТА ОКСИДЫ: гемиоксид N2O и монооксид NO (бесцветные газы), сесквиоксид N2O3 (синяя жидкость), диоксид NO2 (бурый газ, при обычных условиях смесь NO2 и его димера N2O4), оксид N2O5 (бесцветные кристаллы). N2O и NO несолеобразующие оксиды, N2O3… … Энциклопедический словарь
ДИОКСИД — ДИОКСИД, а, муж. (спец.). Химическое соединение, в к ром один атом какого н. элемента соединён с двумя атомами кислорода. Д. азота. | прил. диоксидный, ая, ое. Толковый словарь Ожегова. С.И. Ожегов, Н.Ю. Шведова. 1949 1992 … Толковый словарь Ожегова
АЗОТА ОКСИДЫ — соединения азота с кислородом. Гемиоксид (веселящий газ) N2O газ с приятным запахом; хорошо растворим в воде; tкип 88,5 оС; применяется как анестезирующее средство. Оксид NO газ, плохо растворимый в воде; tкип 151,6 оС; промежуточный продукт в… … Большой энциклопедический политехнический словарь
Безопасность
Быстрое выделение газообразного азота в замкнутом пространстве может вытеснить кислород, и, следовательно, существует угроза удушья. Симптомы «отравления» – сонливость, возникающая из-за гипоксии.
Если газ вдыхают при больших парциальных давлениях, то азот начинает действовать в качестве анестезирующего средства. Это может привести к азотному наркозу и временному легкому опьянению (аналогичным действием обладает закись азота – «веселящий газ»).
Азот растворяется в крови и жирах организма. Быстрая декомпрессия может привести к кессонной болезни, когда пузырьки азота образуются в крови, нервах, суставах и других чувствительных или важных областях. Пузырьки других «инертных» газов (за исключением углекислого газа) оказывают аналогичное воздействие, поэтому замена азота в дыхательных газах может предотвратить азотный наркоз, но не мешает развитию декомпрессионной болезни.
Прямой контакт кожи с жидким азотом вызывает серьезные обморожения (криогенные «ожоги»). Нахождение в природе
Азот является важным строительным блоком аминокислот и нуклеиновых кислот, необходимых для жизнедеятельности на Земле. Он составляет 78% атмосферного воздуха (кислород занимает лишь 21%, все остальное – другие газы).
Распад организмов и их отходов может производить небольшое количество нитрата, но большая часть азота в конечном итоге возвращается в атмосферу. Циркуляция азота из атмосферы к органическим соединениям, а затем обратно в атмосферу, называется азотным циклом.
ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
1. ТЕХНИЧЕСКИЕ ТРЕБОВАНИЯ
1.1. По физико-химическим показателям газообразный и жидкий азот должен соответствовать нормам, указанным в табл.1.
Таблица 1
|
Наименование показателя |
Норма для марки газообразного и жидкого азота |
|||||
|
особой чистоты |
повышенной чистоты |
технического |
||||
|
1-й сорт |
2-й сорт |
1-й сорт |
2-й сорт |
1-й сорт |
2-й сорт |
|
|
1. Объемная доля азота, %, не менее |
99,999 |
99,996 |
99,99 |
99,95 |
99,6 |
99,0 |
|
2. Объемная доля кислорода, %, не более |
0,0005 |
0,001 |
0,001 |
0,05 |
0,4 |
1,0 |
|
3. Объемная доля водяного пара в газообразном азоте, %, не более |
0,0007 |
0,0007 |
0,0015 |
0,004 |
0,009 |
Выдер-живает испыта-ние по п.3.6 |
|
4. Содержание масла в газообразном азоте |
Не определяется |
Выдерживает испытание по п.3.7 |
||||
|
5. Содержание масла, механических примесей и влаги в жидком азоте |
Выдерживает испытание по п.3.8 |
|||||
|
6. Объемная доля водорода, %, не более |
0,0002 |
0,001 |
Не нормируется |
|||
|
7. Объемная доля суммы углеродсодержащих соединений в пересчете на СН, %, не более |
0,0003 |
0,001 |
То же |
Примечания:
1. Показатель по подпункту 1 таблицы включает примеси инертных газов (аргон, неон, гелий).
2. По согласованию с потребителем в техническом газообразном азоте 1-го сорта, транспортируемом по трубопроводу, допускается объемная доля водяного пара более 0,009%.
3. Допускается уменьшение количества жидкого азота вследствие его испарения при транспортировании и хранении не более чем на 10%.
4. Газообразный технический азот, предназначенный для авиации, следует выпускать с объемной долей водяного пара не более 0,003%. Для остальных показателей нормы должны быть не ниже соответствующих норм для технического азота 2-го сорта.
5. На воздухоразделительных установках низкого давления Кт-12, КтК-35, Кт-5 и др. и на установке Кт-3600 разрешается получать жидкий технический азот с объемной долей азота не менее 97,0%.(Измененная редакция, Изм. N 2, 3).
1.2. Коды ОКП технического газообразного и жидкого азота, а также газообразного и жидкого азота особой чистоты приведены в табл.1а.
Таблица 1а
|
Наименование продукта |
Код ОКП |
|
Азот газообразный технический компримированный: |
21 1412 0100 |
|
первый сорт |
21 1412 0130 |
|
второй сорт |
21 1412 0140 |
|
Азот газообразный технический несжатый: |
21 1412 0300 |
|
первый сорт |
21 1412 0330 |
|
второй сорт |
21 1412 0340 |
|
Азот жидкий технический: |
21 1412 0200 |
|
первый сорт |
21 1412 0230 |
|
второй сорт |
21 1412 0240 |
|
Азот газообразный особой чистоты: |
21 1412 0400 |
|
первый сорт |
21 1412 0430 |
|
второй сорт |
21 1412 0440 |
|
Азот жидкий особой чистоты: |
21 1412 0500 |
|
первый сорт |
21 1412 0530 |
|
второй сорт |
21 1412 0540 |
|
Азот газообразный повышенной чистоты: |
21 1412 0700 |
|
первый сорт |
21 1412 0730 |
|
второй сорт |
21 1412 0740 |
|
Азот жидкий повышенной чистоты: |
21 1412 0800 |
|
первый сорт |
21 1412 0830 |
|
второй сорт |
21 1412 0840 |
(Измененная редакция, Изм. N 3).
Немного истории открытия азота
| Внешний вид вещества | |
|---|---|
|
Жидкий азот. При н.у. — газ без цвета, вкуса и запаха. |
|
| Свойства атома | |
| Имя, символ, номер | Азот / Nitrogenium (N), 7 |
| Атомная масса (молярная масса) |
14,00674 а. е. м. (г/моль) |
| Электронная конфигурация | 2s2 2p3 |
| Радиус атома | 92 пм |
| Химические свойства | |
| Ковалентный радиус | 75 пм |
| Радиус иона | 13 (+5e) 171 (-3e) пм |
| Электроотрицательность | 33,04 (шкала Полинга) |
| Степени окисления | 5, 4, 3, 2, 1, 0, −1, −3 |
| Энергия ионизации (первый электрон) |
1401,5 (14,53) кДж/моль (эВ) |
| Термодинамические свойства простого вещества | |
| Плотность (при н. у.) | 0,808 г/см3 (−195,8 °C); при н.у. 0,001251 г./см3 |
| Теплота плавления | (N2) 0,720 кДж/моль |
| Температура кипения | 77,4 K |
| Теплота испарения | 0,904 кДж/моль |
| Молярная теплоёмкость | 29,125(газ N2) Дж/(K·моль) |
| Молярный объём | 17,3 см3/моль |
| Кристаллическая решётка простого вещества | |
| Структура решётки | кубическая |
| Параметры решётки | 5,661 Å |
| Прочие характеристики | |
| Теплопроводность | (300 K) 0,026 Вт/(м·К) |
Генри Кавендишем еще в 1772 году был осуществлен интересный эксперимент, позволивший выделить новое простое вещество — азот. Исследователь выделил азот, но не сумел его распознать. Эксперимент заключался в следующем: над раскаленным углем многократно пропускался воздух, который впоследствии обрабатывался щелочью. Такие манипуляции позволили ученому выделить остаток, который им был определен, как мефитический или удушливый воздух.
Если рассматривать данный эксперимент с точки зрения современной химии, можно прийти к выводу, что кислород, находящийся в потоке воздуха, вступая в реакцию с раскаленным углем, связывался в углекислый газ. Щелочь, которая была задействована на следующем этапе эксперимента, поглощала полученное углекислое соединение. Таким образом, можно прийти к простому выводу, что полученный остаток в большей своей части являлся азотом, который экспериментатор сумел путем достаточно простых действий выделить из атмосферного воздуха.
Не сумев правильно установить полученное вещество, Генри Кавендиш в том же 1772 году сообщил о результатах своей работы Джозефу Пристли, который в то же самое время работал над решением аналогичной задачи. Он осуществлял эксперименты, намереваясь связать кислород и удалить полученный, таким образом, углекислый газ. Джозеф Пристли в те времена являлся приверженцем теории флогистона. Соответственно, он абсолютно неправильно истолковывал получаемые результаты и был абсолютно уверен в том, что не кислород вытесняется из воздуха, а наоборот. Пристли не сомневался, что в процессе производимых им манипуляций происходит насыщение воздуха флогистоном. Таким образом, он именовал оставшийся воздух (то есть практически азот) флогистированным, что означало — насыщенным флогистоном.
Оба эти экспериментатора хоть и нашли способы выделить из воздуха азот, но не считаются его первооткрывателями вследствие ошибочного толкования результатов своей деятельности. Карл Шееле в те же времена занимался аналогичной деятельностью, а Даниэль Резерфорд все в том же 1772 году опубликовал магистерскую диссертацию, в которой упомянул азот, используя термин «испорченный воздух». Резерфордом в своей научной работе были указаны основные свойства азота. Им абсолютно верно было установлено следующее:
- отсутствие взаимодействия полученного газа со щелочами;
- непригодность использования его для дыхания;
- выделенный газ не поддерживает горения.
В связи с верными выводами именно Даниэля Резерфорд многие признали первооткрывателем азота. К сожалению, он также, как и Джозеф Пристли был приверженцем флогистонной теории, поэтому так и не смог осознать, что именно за вещество ему удалось выделить из обычного атмосферного воздуха. Анализируя все вышесказанное, можно прийти к выводу, что точно определить, кто же именно открыл азот, не представляется возможным. Азот и далее подвергался исследованию многими учеными, которые все-таки со временем определили полный спектр его характеристик, что позволило в наши дни использовать данный газ во многих сферах профессиональной деятельности человека.
Конструктивные особенности изотермической цистерны для транспортировки жидкого азота:
- цистерна для перевозки охлажденного до состояния жидкости азота имеет цилиндрическую форму, сварную многослойную конструкцию с вакуумной или объемной термоизоляцией;
- внешний кожух выполнен из стали, промежуточный слой составляют вакуум и огнеупорные изоляционные материалы, внутри размещен сосуд для перевозимого вещества;
- для дополнительной защиты от прямых солнечных лучей внешняя поверхность резервуара окрашивается в светлые тона, накрывается специальным чехлом;
- внутренний сосуд рассчитан на эксплуатацию при избыточном давлении;
- манометры, датчики температуры, запорная арматура, предохранительный клапан давления размещены в специальном люке в задней части цистерны;
- арматура для налива/слива предусмотрена в нижней части цистерны;
- цистерна снабжена уровнемером поплавкового типа.
Специальные требования к резервуарам для перевозки криогенных веществ – наличие техпаспорта, обязательная регистрация в Ростехнадзоре.
Физические характеристики вещества
В нормальных условиях (при атмосферном давлении 760 мм рт. ст. и температуре 0°С) вещество представляет собой газ без запаха и цвета, который плохо растворяется в воде. Он не вступает в реакции с другими элементами за исключением лития. При нагревании азот приобретает способность к диссоциации на атомы и создает различные химические соединения. Наиболее востребована его реакция с водородом, в результате которой получается аммиак, используемый для изготовления удобрений, хладагента, синтетических волокон и пр. Газообразный азот пожаро- и взрывобезопасен, к тому же он препятствует гниению и окислению. Вещество нетоксично, поэтому не оказывает опасного влияния на окружающую среду. Но при длительном вдыхании вызывает кислородную недостаточность и удушье.
При охлаждении до -195,8°С азот превращается в жидкость, напоминающую по внешнему виду обычную воду. Температура кипения данного вещества несколько ниже, чем у кислорода. Поэтому при нагревании жидкого воздуха азот начинает испаряться первым. Данное свойство лежит в основе современного принципа производства химического продукта. Многократное повторение сжижения и вскипания дает возможность получить азот и кислород в нужной концентрации. Данный процесс получил название ректификации.
Если азот в жидком состоянии, объем которого составляет 1 литр, нагревать до +20°С, он будет испаряться и образует 700 литров газа. Поэтому вещество хранят в специальных емкостях открытого типа с вакуумной изоляцией либо в криогенных сосудах под давлением.
Последующее охлаждение азота до -209,86°С переводит его в твердое агрегатное состояние. Получаются большие белоснежные кристаллы. При последующем контакте с воздухом снегоподобная масса поглощает кислород и плавится.
Токсичность и опасность
Воздух рабочей зоны
| ПДК максимальная разовая, мг/м3 | 2 |
| Класс опасности | 3 |
| Особенности токсического действия вещества на организм | остронаправленный механизм действия, требующий автоматического контроля за содержанием вещества в воздухе (О) |
Атмосферный воздух населённых мест
| ПДК максимальная разовая, мг/м3 | 0,2 |
| ПДК среднесуточная, мг/м3 | 0,04 |
| Класс опасности | 3 |
| Лимитирующий показатель вредности | Рефлекторно-резорбтивный |
Аварийные гигиенические регламенты и референтные уровни
| Уровни острой ингаляционной
экспозиции (мг/м³) |
|
||||||||||||||||||||||||
| Аварийные пределы воздействия
отравляющих веществ в воздухе (АПВ, мг/м³) |
|
||||||||||||||||||||||||
| Референтные концентрации для
хронического ингаляционного |
0,04 | ||||||||||||||||||||||||
| Поражаемые органы и системы | органы дыхания, кровь (образование MetHb) | ||||||||||||||||||||||||
| Субъективная реакция дискомфорта (мг/м³) |
0,25 |
Опасность при утечке
Вещество может всасываться в организм при вдыхании и через рот. При утечке содержимого очень быстро достигается опасная концентрация этого газа в воздухе. Вещество раздражает глаза, кожу и дыхательные пути. Вдыхание газа или пара может вызвать отек легких. Воздействие на высоком уровне может вызвать смерть. Эффекты могут быть отсроченными. Вещество является сильным окислителем и бурно реагирует с горючими материалами и восстановителями. Реагирует с водой с образованием азотной кислоты и оксида азота. Агрессивно в отношении стали в присутствии влаги.
Острая токсичность
| Токсичность для животных |
|
||||||||
|
Токсичность для человека |
| Тип дозы | Способ измерения | Механизм воздействия | Состояние человека | Значение |
|---|---|---|---|---|
|
Наименьшая опубликованная смертельная доза (LCLo, LDLo) |
в целом на организм | ингаляционно | в состоянии покоя | 376 (1 мин) мг/м3 |
| Наименьшая опубликованная токсичная доза (TCLo, TDLo) | в целом на организм | ингаляционно | в состоянии покоя | 3,8 мг/м3 |
| Наименьшая опубликованная токсичная доза (TCLo, TDLo) | в целом на организм | ингаляционно | в состоянии покоя | 169 (40 мин) мг/м3 |
| Мгновенно-опасная для жизни или здоровья концентрация (IDLH) | в целом на организм | ингаляционно | в состоянии покоя | 37,6 мг/м3 |
| Пороговая токсодоза (PCt50, мг.мин/л) | 4,2 |
| Смертельная токсодоза (LCt50, мг.мин/л) | 58,3 |
Автомобильная транспортировка азота

Перевозка жидкого Азота
Жидкий азот в малых количествах общим объемом до 1000 м3 разрешено перевозить автомобильным транспортом в баллонах специальной конструкции (сосудах дьюара) без основных ограничений, предъявляемых к транспортировке опасных грузов.
Основные требования, предъявляемые к оборудованию и комплектации автотранспорта, предназначенного для перевозки опасных грузов, прописаны в ДОПОГ.
- Все тягачи и прицепы обязаны иметь действующее свидетельство о допуске к перевозке опасных веществ, дважды в год проходят техосмотр, в ходе которого получают диагностическую карту о пригодности и возможности дальнейшего использования.
- Автотранспортные средства, предназначенные для транспортировки грузов повышенной опасности, в том числе легковоспламеняющихся сжиженных газов в цистернах под давлением, должны быть включены в Реестр категорированных объектов транспортной инфраструктуры и средств Федерального дорожного агентства.
- Согласно приказу Минтранса №20 автомобили, перевозящие опасные грузы должны иметь в оснащении аппаратуру спутниковой навигации (GPS или ГЛОНАСС), тахографы.
- Обязательно проходят предрейсовый и послерейсовый техосмотр.
- Дополнительно транспортное средство для перевозки горючих газов должно иметь защиту топливного бака, установленные проблесковые маячки оранжевого цвета, дополнительные фонари (оранжевые) с автономным питанием и защитным кожухом.
Автомобиль и прицеп обязательно маркируются соответствующими знаками опасности:
- Впереди на тягаче обязательно крепится информационная табличка оранжевого цвета, содержащая вверху идентификационный номер опасности – 22, внизу – порядковый номер ООН 1977 (жидкий азот);
- сзади на цистерне, кузове помещается аналогичная табличка и знак опасности согласно правилам маркировки горючих газов: ромб оранжевого цвета, вверху — пламя над окружностью, внизу номер класса — 2.
Экипаж транспортного средства должен пройти обучение, быть аттестован по программе ДОПОГ для соответствующего класса опасных грузов, о чем свидетельствует наличие удостоверения. При транспортировке криогенных веществ, водителям требуется дополнительная экипировка: криогенные перчатки, антистатическая одежда, специальная обувь, каска, наушники, очки.
Диоксид азота
Источники
Выхлопные газы автомобилей, выбросы ТЭЦ, сжигание твердых отходов, сгорание газа. Также преобразуется из NO при реакции с кислородом
Дыхательные пути
При небольших концентрациях диоксида азота наблюдается нарушение дыхания, кашель. При длительном действии оксидов азота следует опасаться расширения клеток в корешках бронхов.
Легкие
При контакте с влагой в организме образуются азотистая и азотная кислоты, которые разъедают стенки альвеол легких. При этом, стенки альвеол и кровеносных капилляров становятся настолько проницаемы, что пропускают сыворотку крови в полость легких. В этой жидкости растворяется вдыхаемый воздух, образуя пену, препятствующую дальнейшему газообмену. Ухудшает сопротивляемость легких к бактериям, что снижает общую сопротивляемость организма к заболеваниям.
Общее воздействие
При длительном вдыхании этого газа происходит кислородное голодание тканей, особенно у детей. Вызывает болезни, кровообращения и злокачественные новообразования. Обладает токсичностью, негативно воздействует на генетический материал, репродуктивные органы, глаза, кожный покров. Оказывает сильное действие на центральную нервную систему.
Почва
При взаимодействии с влагой во время дождя N02 превращается в азотную кислоту, которая увеличивает кислотность почвы.
Растения
Длительное воздействие диоксида азота в концентрации 0,47-1,88 мг/м3 может подавлять рост некоторых растений. Оксиды азота действуют на растения двумя путями: с помощью кислотных осадков, прямым контактом с растениями, и косвенно путем фотохимического образования окислителей. В форме кислотных остатков оксиды азота наносят ущерб растениям, увеличивая кислотность. Прямой контакт растений с оксидами азота можно зрительно определить по пожелтению или по бурению листьев и игл. Образующаяся в клетках азотистая кислота оказывает мутагенное действие, выражающееся в нарушениях хромосомного аппарата и проявлениях наследственных уродств.
Диоксид азота играет важную роль в образовании фотохимического смога, который значительно ухудшает видимость и портит эстетику окружающей среды в целом.