Гост 2604.8-77. чугун легированный. методы определения никеля (с изменениями n 1, 2)
Содержание:
- 13. КОНТРОЛЬ КАЧЕСТВА РЕЗУЛЬТАТОВ АНАЛИЗА ПРИ РЕАЛИЗАЦИИ МЕТОДИКИ В ЛАБОРАТОРИИ
- Статья составлена с использованием следующих материалов:
- Текст
- Реакционная способность
- 3. СРЕДСТВА ИЗМЕРЕНИЙ. ВСПОМОГАТЕЛЬНОЕ ОБОРУДОВАНИЕ. МАТЕРИАЛЫ, РЕАКТИВЫ
- Диметилглиоксимат — никель
- Методы синтеза
- Применение
- ГРАВИМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ НИКЕЛЯ ОСАЖДЕНИЕМ ДИМЕТИЛГЛИОКСИМОМ
- 7. ОТБОР И ХРАНЕНИЕ ПРОБ ВОДЫ
13. КОНТРОЛЬ КАЧЕСТВА РЕЗУЛЬТАТОВ АНАЛИЗА ПРИ РЕАЛИЗАЦИИ МЕТОДИКИ В ЛАБОРАТОРИИ
Контроль качества результатов анализа при реализации методики в лаборатории предусматривает:
— оперативный контроль процедуры анализа (на основе оценки погрешности при реализации отдельно взятой контрольной процедуры);
— контроль стабильности результатов анализа (на основе контроля стабильности среднеквадратического отклонения повторяемости, среднеквадратического отклонения внутрилабораторной прецизионности, погрешности).
Алгоритм оперативного контроля процедуры анализа с использованием метода добавок
Оперативный контроль процедуры анализа проводят путем сравнения результата отдельно взятой контрольной процедуры Ккс нормативом контроля К.
Результат контрольной процедуры Кк рассчитывают по формуле
где Х′ср — результат анализа массовой концентрации никеля в пробе с известной добавкой — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию () раздела .
Хср — результат анализа массовой концентрации никеля в исходной пробе — среднее арифметическое двух результатов параллельных определений, расхождение между которыми удовлетворяет условию () раздела .
Норматив контроля К рассчитывают по формуле
где , — значения характеристики погрешности результатов анализа, установленные в лаборатории при реализации методики, соответствующие массовой концентрации никеля в пробе с известной добавкой и в исходной пробе соответственно.
Примечание. Допустимо характеристику погрешности результатов анализа при внедрении методики в лаборатории устанавливать на основе выражения: Δл = 0,84 × Δ, с последующим уточнением по мере накопления информации в процессе контроля стабильности результатов анализа.
Процедуру анализа признают удовлетворительной, при выполнении условия:
Кк£ К ()
При невыполнении условия () контрольную процедуру повторяют. При повторном невыполнении условия () выясняют причины, приводящие к неудовлетворительным результатам, и принимают меры по их устранению.
Периодичность оперативного контроля процедуры анализа, а также реализуемые процедуры контроля стабильности результатов анализа регламентируют в Руководстве по качеству лаборатории.
Статья составлена с использованием следующих материалов:
БуклетZELLEKSUPER, EC / ЗЕЛЛЕК-СУПЕР, КЭ. Dow AgroSciences / ДауАгроСаенсес
2.
Гигиенические нормативы содержания пестицидов в объектах окружающей среды (перечень). Гигиенические нормативы ГН 1.2.2701-10  Скачать >>>
3.
Государственный каталог пестицидов и агрохимикатов, разрешенных к применению на территории Российской Федерации, 2013 год. Министерство сельского хозяйства Российской Федерации (Минсельхоз России)
4.Мельников Н.Н. Пестициды. Химия, технология и применение. — М.: Химия, 1987. 712 с.
5.
Новожилов К.В. Долженко В.И. Средсва защиты расений. – М., 2011. – 244 с.
6.
Определение остаточных количеств Галоксифопа-Р-метила и Галоксифопа-Р в воде, Галоксифопа-Р в почве, зеленой массе растений, клубнях картофеля, корнеплодах сахарной, кормовой и столовой свеклы, семенах и масле льна, рапса, сои, подсолнечника методом газожидкостной хроматографии. Методические указания. МУК 4.1.2163-07
7.
Ракитский В.Н. Справочник по пестицидам (токсиколого-гигиеническая характеристика). Выпуск 1. Под редакцией академика РАМН В.Н. Ракитского. – М.: Издательство Агрорус, 2011. – 960 с.
Свернуть
Список всех источников
Текст
:);:ькц 2- 5 ачт»550 г. 3 Л. 1 чь». ц слсОЯ у к.;РИЗВЕСТНЫЕ СПОСООЬ ПОЛ ЧЕНИ 51;И)ЕТНЛГ)ИОКСИ.Я ОСНОВАНЫ Н пиРОЗирОВянии ъетилзтялкетоя 11;Оссд 0 цс 51 Оксн)пп)овапнн Обр;1- ЗуОЩсг 0051 диаЦстилзОнооксн)12, Однако, недостатка)и этн); способоВ 5 В,151 стс 5 На;ппе побочы процессов, 5 рвод 5 щп.; и ос)олени 0 дпаце)илоноокси)а, и невысокГй выкод д: метилглиоксима.-,.-.- — Я )Ь С,ОСОО: СЛГЧС):15. Д)С.:.Л ГЛ:О С:Л 2 СТРЯНЯСТ указаныс недостатки и даст ВОзможность получ 1 ь чистыЙ ди)сти,- Г, 15 ОКСИ, » 00:1 ЕЕ В 1 СОКИ. ВЫ:ДО).Отличие описывае 5 ого способа от известнык закгпочаеся в то.;к что нитрозирова ие ведт в Ваствоое )стянол плп этапола до тсоост;- ЧЕСКИ ВЫЧИСЛЕННОГО 1 РИВССЯ; РЯСТГ)Р ГИДРОКСИ,12:5 ННДИСУэфо 1 Т .Ятри 5 В ц,.5. :.:;,Олк;я:;: р,заот:,. . Оке:):,НИ 1:.с, 3 цс,15 АС ф)», НЕНИ О, 0,1051,5 д)О.3; 0.550)Я 31 С., .:РТОЗО 0 )1 СТВО,) Я Д: )ет 5 Л)оноокс.) к пол «;».».:О.:», и Ол к:с:но)у дд -. — -)5 гидроссила)Иносульфопата. Г 1 р и )е р 1. Нитрозрование )етлэтплкетона, 90: .;етилэтилкетона сешпваот с 00; Оезводно 0 5 ет,ОВОГО спирта и 15,я. концентрирсванноц сол 5 но кислоты, нагревают до, . о 40 — )О и нит 1)03 ротп;)с 1. сна 1 3 .ет;лзт:лкстс 51 Газооор, Зпып 1 =Г:,- нитрит, по;1 ученеыЙ путе)1:10 дкпслепия 51 -:0 ОерноЙ кс,1 ОтОЙ ВОнс)- спиртового раствора 105 г натрия В 150 32 этилового спи)та и 861 5 ил ВОды. Те)ператур 1 нптроз,)Овани 51 40 — ,5:оддср)КиваОт путе) Всп. ГГО Оъляждения Водой .етплспртОВОГО рястВОра )стп,этп;1 кстоня. КО;,сц итрОЗирогания Опрс.;е,яют по увслпОни 0 Об)ьс».Я /)еакц;онпо 0 растВОрЯ див петил);Онооксма до )68 — )68 ял, 1 😉 сООтве)с Гвует привссу 80 — 82 г или 106 — 109″а ст тсорпп, сч;тая на этп,шГрп. П 1) и . е р . Окси,ирсванис диацсти,.10100 ксп.а.175 г текничсского 08″,о-ного нитрпта 1;атрия растворяют в 1.5 л воды. К водному раствору нитритя при размешиван 5 и в течение 1 — 2″.55 и. приливают 1,15 . 86 а-ного стандартного раствора бисульфчт. Натрия. Пол енньп пастзор Гпд)оксила:и дискьфоната н)тпи 588851 Предмет из о бр е т ения 1. Способ по;гучения дихечслг)гг(ио(ксиа путем питрознрования метилэтилкетона эфирами азотистой кислоты и 1;оследующего оксимирования образующегося диацеиилмонооксима с применением гидрокспламиндисульфоната натрия, о тл и ч а ю щи й с я тем, что нитрозирование ведут в растворе метанола или эта(к)ла до теоретически вычисле)(- ного привеса.2, Прием выполнен(ия сгособа по п. 1, отличающийся тем, что раствор Гидроксилауиндису,(пэОИ 5)та натрия, В целях ускореи 5 1 идролиза, нагревают до 100.3. Прием выполнения способа по п. 1, о(т л и ч а ю щи й с я тем, что оксимирование, в целях устраненИя осмоления, производят приоавлением спиртового раствора диацети,гмонсоксима к раствору гидроксил. аминосульфоната, получаемому по и. 2, охг(аждс(иному до 40 — 45. комитет ио делам изоб)втеки) и открти) и)гн Совете Ы)(пиетров СССР 1 едактор А, К. Ле)1 ки)ш) Поди. к иеп. З Х о=а тТираж 360. Цена 25 коп,Информационно-издательский отдел,Объем 0,17 и. л. За, 1 Ь:). Гор. Алатырь, типографпп 2 Мини(терства культуры Еувашской АССР. Ох,)кЯ)к)т:О 20 и (ОдкР(с 5)О рс)зО)Б,(сноп 30″,а-О) (ср0) к)(с;)О- Той до слабок 5)сг)ой реакции на кого и нагревают до 100. 11 осл( охлаждения до 40 к полученному водному раствору гидроксиламинсульфоната натрия прибавляют при размешиванпи 2 б 1 — 2 б 4 лл спиртового раствора диацетилмонооксима )и нагревают при 40 — 50 в течение 3 час, Выпадение диметилглиоксима происходе(т через 0,5 часа после нагревания реакционной смеси и заканчивается через 20 — 24 часа. Выпавш(ий д)иметилглиокси) отфильтровывают от маточника, промывают водой от ионов серной кислоты и сушат до постоянного веса. Получают 87 — 88,5 г димстилглиоксима, что соответствует 7475) От теоретического,
Смотреть
Реакционная способность
Оксимы проявляют амфотерные свойства, являясь как очень слабыми основаниями, так и слабыми кислотами (pKa ~ 11, pKb ~ 12).
Оксимы под действием алкоголятов щелочных металлов депротонируются, образуя соответствующие соли, они также могут образовывать соли с переходными металлами, в последнем случае возможно комплексообразование, особенно в случае бидентантных оксимов. Так, например, диметилглиоксим (реактив Чугаева) образует с двухвалентным никелем прочный нерастворимый комплекс; эта реакция используется для гравиметрического определения никеля.
Оксимы являются амбидентантными нуклеофилами, способными алкилироваться и по атому кислорода, и по атому азота: так, соли оксимов с щелочными металлами алкилируются алкилгалогенидами с образованием O-алкилоксимов:
- RR1C=NOH + C2H5ONa →{\displaystyle \to } RR1C=NONa + C2H5OH
- RR1C=NONa + R2I →{\displaystyle \to } RR1C=NOR2 + NaI
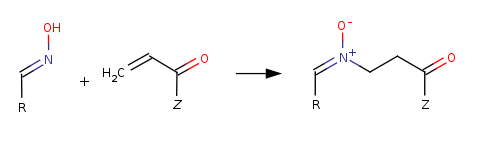
Алкилирование может идти и по атому азота, в этом случае образуются нитроны, к образованию нитронов ведет также присоединение к оксимам α,β-ненасыщенных карбонильных соединений:
Энергичными восстановителями оксимы восстанавливаются до аминов, также возможно восстановление до N-замещенных гидроксиламинов.
Оксимы дегидрируются с образованием иминоксильных радикалов:
- R2C=NOH →{\displaystyle \to } R2C=N-O•
Под действием перокситрифторуксусной кислоты, получаемой in situ из трифторуксусного ангидрида и перекиси водорода оксимы окисляются до нитросоединений; в случае циклогексаноноксима реакцию проводят в кипящем ацетонитриле в присутствии буфера, при окислении оксимов α-дикетонов в α-нитрокарбонильные соединения в качестве растворителя может быть использован хлороформ или трифторуксусная кислота, необходимости в буфере в этом случае нет, предполагается, что первоначально образуется аци-форма нитросоединения, которая затем таутомеризуется:
- RCOCR=NOH + CF3COOOH →{\displaystyle \to } RCOCR=NO(OH) →{\displaystyle \to } RCOCHRNO2
N-бромсукцинимид (NBS) реагирует с оксимами с образованием соответствующего гем-бромнитрозопроизводного:
- R2C=NOH + NBS →{\displaystyle \to } R2CBr(NO)
Под действием азотной кислоты кетоксимы дают гем-нитронитрозосоединения (псевдонитролы):
- R2C=NOH + HNO3→{\displaystyle \to } R2CNO(NO2) ,
альдоксимы нитруются до изомерных (и, в случае альдоксимов и таутомерных) псевдонитролам нитроловых кислот:
- RCH=NOH + HNO3→{\displaystyle \to } R(CO)C(NO2)=NOH + H2O
Ароматические альдоксимы хлорируются с образованием гидроксамоилхлоридов (хлорангидридов иминных таутомеров гидроксамовых кислот, которые, в свою очередь, могут быть превращены в оксиды нитрилов:
- Ph-CH=NOH + Cl2→{\displaystyle \to } Ph-CCl=NOH + HCl
- Ph-CCl=NOH + Et3N →{\displaystyle \to } Ph-C≡N+-O-
Под действием кислотных и ацилирующих агентов (PCl5, P2O5, полифосфорные кислоты, хлорангидриды сульфокислот и карбоновых кислот) альдоксимы отщепляют воду с образованием нитрилов:
- RCH=NOH + Ac2O →{\displaystyle \to } RCN + 2 AcOH
Кетоксимы в таких условиях перегруппировываются в амиды (Перегруппировка Бекмана), перегруппировка стереоспецифична — к азоту мигрирует радикал, находящийся в транс-положении к гидроксилу:
- RR1C=NOH →{\displaystyle \to } RCONHR1
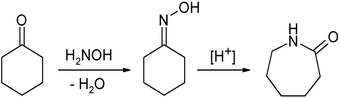
Перегруппировка Бекмана циклогексаноноксима является промышленным методом синтеза капролактама — мономера капрона (найлона-6):
Перегруппировку Бекмана также претерпевают O-замещённые кетоксимы (сложные эфиры оксимов, перегруппировка Бекмана-Чепмена):
- RR1C=NOR2→{\displaystyle \to } RCONR1R2
Перегруппировка Бекмана может проходить и под действием P2S5, выступающего в роли и катализатора перегруппировки, и тионирующего агента, продуктом реакции в этом случае являются тиоамиды. Так, бензальдоксим в этих условиях образует тиобензамид:
- PhCH=NOH + P2S5→{\displaystyle \to } PhCSNH2 ,
бензофеноноксим перегруппировывается в тиобензанилид:
- (Ph)2C=NOH + P2S5 PhCSNHPh
α-Гидроксикетоксимы в условиях перегруппировки Бекмана расщепляются с образованием альдегида и нитрила (расщепление по Бекману или перегруппировка Вернера):
- RCH(OH)CR1=NOH →{\displaystyle \to } RCHO + R1CN + H2O
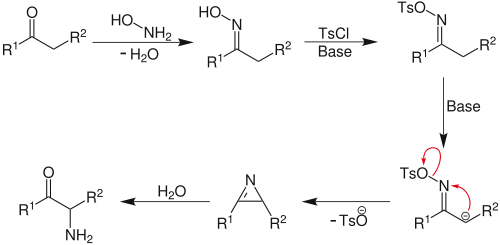
O-сульфонаты оксимов алифатических кетонов под действием оснований претерпевают перегруппировку, образуя азирины, гидролизующиеся далее до α-аминокетонов (перегруппировка Небера), эта реакция является синтетическим методом α-аминирования кетонов:
3. СРЕДСТВА ИЗМЕРЕНИЙ. ВСПОМОГАТЕЛЬНОЕ ОБОРУДОВАНИЕ. МАТЕРИАЛЫ, РЕАКТИВЫ
3.1. Средства измерений, вспомогательное оборудование
Спектрофотометр или фотоэлектроколориметр, позволяющий измерять оптическую плотность при длине волны λ = 445 нм.
Кюветы с толщиной поглощающего слоя 10 и 50 мм.
Весы лабораторные 2-го класса точности по ГОСТ 24104.
Сушильный шкаф электрический, ОСТ 16.0.801.397.
Плитка электрическая по ГОСТ 14919.
ГСО с аттестованным содержанием никеля с погрешностью не более 1 %.
3.2. Посуда
Колбы мерные 2-25 (50, 100)-2 по ГОСТ 1770.
Пипетки мерные 6(7)-1(2, 5, 10) по ГОСТ 29227
Воронки делительные ВД-1-250 ХС по ГОСТ 25336.
Колбы конические К-2-100(200)-34 ТХС по ГОСТ 25336.
Стаканы для взвешивания Н-1-50 ТХС по ГОСТ 25336.
Чашки фарфоровые выпарительные 3(4) по ГОСТ 9147.
Бутыли из стекла или полиэтилена с притертыми или винтовыми пробками вместимостью 250 — 500 см3 для отбора и хранения проб.
3.3. Реактивы, материалы
Аммиак водный по ГОСТ 3760.
Диметилглиоксим по ГОСТ 5828.
Перекись водорода (30 %-ный водный раствор) по ГОСТ 10929.
Спирт этиловый ректификованный технический по ГОСТ 18300.
Серная кислота по ГОСТ 4204.
Азотная кислота по ГОСТ 4461.
Соляная кислота по ГОСТ 3118.
Калий-натрий виннокислый, (сегнетова соль) по ГОСТ 5845.
Аммония персульфат по ГОСТ 20478.
Хлороформ ТУ 6-09-06-800 (перегнанный).
Гидроксиламина гидрохлорид по ГОСТ 5456.
Метиловый оранжевый индикатор по ГОСТ 10816.
Бром по ГОСТ 4109.
Натрий гидроксид по ГОСТ 4328.
Вода дистиллированная по ГОСТ 6709.
Бумага индикаторная универсальная, ТУ 6-09 1181.
Все реактивы должны быть квалификации ч.д.а. или х.ч.
Диметилглиоксимат — никель
Осадок диметилглиоксимата никеля, полученный на холоду из щелочного раствора, обычно рыхлый. Поэтому осаждение ведут из нагретого до 40 — 45 слабокислого раствора, кислоту затем нейтрализуют аммиаком. Нагревать раствор при осаждении до более высокой температуры не рекомендуется, так как возможна неполнота осаждения.
Осадок диметилглиоксимата никеля, полученный на холоду из щелочного раствора, обычно рыхлый. Поэтому осаждение ведут из нагретого до 40 — 45 слабокислого раствора, кислоту затем нейтрализуют аммиаком. Нагревать раствор при осаждении До более высокой температуры не рекомендуется, так как возможна неполнота осаждения.
Осадок диметилглиоксимата никеля обладает весьма ценными для анализа свойствами. Так, он весьма мало растворим в воде ( ПР2 3 — 10 — 25), концентрация ионов Mi 1 в его насыщенном растворе составляет около 4 — 10 — 9 г-ион. Избыток осадителя еще больше понижает эту и без того весьма малую растворимость осадка. Далее, весьма ценно, что осадок получается достаточно чистым. Наконец, реакция довольно специфична. Из других катионов трудно растворимые осадки с диметилглиоксимом дают только палладий и платина, которые редко встречаются при обычном ходе анализа.
Осадок диметилглиоксимата никеля обладает весьма ценными для анализа свойствами. Избыток осадителя еще больше понижает эту и без того весьма малую растворимость осадка. Далее, весьма ценно, что осадок получается достаточно чистым. Наконец, реакция довольно специфична. Из других катионов трудно растворимые осадки с диметилглиоксимом дают только палладий и платина, которые редко встречаются при обычном ходе анализа.
В диметилглиоксимате никеля имеется четыре цикла: два пяти-членных и два шестичленных. Образование шестичленных циклов обусловлено водородной связью.
Полнота осаждения диметилглиоксимата никеля сильно зависит от рН раствора. Получающийся осадок весьма чист, а сама реакция довольно специфична.
Образование осадка диметилглиоксимата никеля происходит медленно.
В структурах диметилглиоксиматов никеля, палладия и платины большую роль играет межмолекулярное взаимодействие между атомами металла соседних молекул.
|
Поляризационные кривые восстановления кислорода на платиновом электроде в 3 N КОН ( / и растворе комплекса, насыщенного кислородом ( 2.| Поляризационные кривые восстановления кислорода, связанного о комплексом, на пористых серебряные электрэд х при разных скоростях подачи электролита. |
В растворах диметилглиоксимата никеля вслед за процессом кксигенации происходит значительно более медленный процесс необратимого окисления. В концентрированных по щелочи растворах ( 6 N) количество обратимо связанного кислорода за первые двое суток уменьшается примерно наполовину. Дальнейшее окисление протекает в течение нескольких суток и сопровождается выпадением осадка. В более разбавленных по щелочи растворах стадия необратимого окисления проходит медленнее. Этот процесс сильно затрудняет изучение основного процесса — окси-тенации и существенно снижает воспроизводимость результатов.
Отфильтровав осадок диметилглиоксимата никеля через бы-строфильтрующий фильтр, растворяют осадок в горячей соляной кислоте ( 1 1), собирая раствор Б стакан, где велось первое осаждение.
Образующийся осадок диметилглиоксимата никеля очень объемистый, поэтому исходный раствор должен содержать около 0 02 г никеля.
Выделившийся осадок диметилглиоксимата никеля отфильтровывают через фильтр ( белая лента), промывают горячей водой, растворяют в горячей 10 % — ной НС1, прибавляют 0 2 — 0 3 г винной ( лимонной) кислоты и вновь осаждают никель диметплглп-оксимом, как и в первый раз.
|
Приспособление для фильтрования с отсасыванием через фильтровальный тигель ( стеклянный или фарфоровый. |
Образующийся осадок диметилглиоксимата никеля очень объемистый, поэтому исходный раствор должен содержать около 0 02 г никеля. Осадок практически нерастворим в разбавленных растворах аммиака, солях аммония, избытке осадителя и в аце-татно-буферных смесях. Он растворим в минеральных кислотах, в растворах цианидов и в спирте.
Методы синтеза
Наиболее распространенным лабораторным методом синтеза оксимов является реакции альдегидов и кетонов с гидроксиламином:
- CH3COCH3 + NH2OH →{\displaystyle \to } CH3(C=N-OH)CH3 + H2O
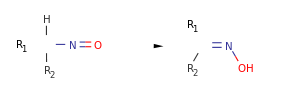
Другим широко используемым методом является изомеризация нитрозосоединений, содержащих водород в α-положении к нитрозогруппе:
Такая изомеризация проходит in situ при нитрозирования некоторых алканов (например, циклогексана нитрозилхлоридом NOCl) или соединений с активированной метильной либо метиленовой группой:
- PhCOCH3 + C5H11ONO →{\displaystyle \to } [ PhCOCH2N=O ] →{\displaystyle \to } PhCOCH=N-OH
Аналогично проходит нитрозирование некоторых замещенных толуолов: нитротолуолы при взаимодействии с алкилнитритами в присутствии алкоксидов образуют соответствуюцие альдоксимы.
Нитрозирование замещенных нитрометанов также приводит к вводу оксимной группы при атоме углерода с образованием геминальных нитрооксимов — нитроловых кислот:
- RCH2NO2 + HNO2→{\displaystyle \to } RC(NO2)=NOH + H2O
Оксимы также могут быть синтезированы окислением первичных аминов:
- RR1CH-NH2 + H2O2→{\displaystyle \to } RR1C=NOH + H2O
либо восстановлением нитросоединений:
- RCH2NO2 + →{\displaystyle \to } RCH=NOH + H2O
Специфическим методом синтеза ароматических оксимов является прямое введение альдоксимной группы в ароматическое ядро конденсацией бензола, его алкилпроизводных и фенолов с фульминатом ртути в присутствии хлорида алюминия:
- C6H6 + Hg(ONC)2→{\displaystyle \to } C6H5CH=NOH
Применение
Галоксифоп-Р-метил рекомендован для борьбы с однолетними и многолетними однодольными сорняками в посевах хлопчатника, сахарной свеклы, риса и других культур как послевсходовый гербицид.
Зарегистрированные препараты на основе галоксифоп-Р-метила применяются против однолетних злаковых сорняков (виды щетинника, просо сорно-полевое, просо куриное) в посевах свеклы сахарной и кормовой, сои, подсолнечника, льна-долгунца; против однолетних и многолетних злаковых сорняков в посевах эхинацеи пурпурной и маклеи сердцевидной 1-го года вегетации, наперстянки шерстистой; однолетних злаковых сорняков, пырея ползучего в посевах рапса.
ГРАВИМЕТРИЧЕСКИЙ МЕТОД ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ НИКЕЛЯ ОСАЖДЕНИЕМ ДИМЕТИЛГЛИОКСИМОМ
3.1. Сущность метода
Метод основан на осаждении никеля диметилглиоксимом в слабоаммиачном растворе (рН 8 — 10). Мешающее влияние железа, хрома, марганца и других элементов устраняют прибавлением винной кислоты. Осадок диметилглиоксимата никеля высушивают и взвешивают.
3.2. Реактивы и растворы
Кислота соляная по ГОСТ 3118-77, разбавленная 1:1 и 1:100.
Кислота азотная по ГОСТ 4461-77.
Кислота серная по ГОСТ 4204-77.
Кислота фтористоводородная по ГОСТ 10484-78.
Калий пиросернокислый по ГОСТ 7172-76.
Аммоний хлористый по ГОСТ 3773-72, 10 %-ный раствор.
Кислота винная по ГОСТ 5817-77, 50 %-ный раствор.
Аммиак водный по ГОСТ 3760-79.
Спирт этиловый ректификованный по ГОСТ 18300-87.
Диметилглиоксим по ГОСТ 5828-77, 1 %-ный спиртовой раствор; готовят следующим образом: 10 г диметилглиоксима растворяют в 750 см3 спирта, приливают 250 см3 горячей воды и перемешивают.
Индикатор универсальный, бумага.
3.3. Проведение анализа
Массу навески чугуна в зависимости от массовой доли никеля определяют по табл. .
Таблица 1
|
Масса навески, г |
|
|
От 0,1 до 0,5 |
3,0 |
|
Св. 0,5 » 2,0 |
2,0 |
|
» 2,0 » 4,0 |
1,0 |
|
» 4,0 » 10,0 |
0,5 |
|
» 10,0 » 25,0 |
0,2 |
Навеску помещают в стакан вместимостью 500 см3, накрывают часовым стеклом и растворяют при умеренном нагревании в 30 см3 соляной кислоты, прибавляя по каплям азотную кислоту до прекращения вспенивания. Раствор выпаривают досуха. К сухому остатку приливают 10 см3 соляной кислоты и снова выпаривают досуха. Затем приливают 10 — 20 см3 соляной кислоты и содержимое стакана нагревают до растворения солей. К раствору приливают 80 — 100 см3 горячей воды, нагревают до 80 — 90 °С, обмывают часовое стекло водой, отфильтровывают выпавший осадок кремниевой кислоты и графит на фильтр «белая лента» с добавлением бумажной массы. Осадок на фильтре промывают несколько раз соляной кислотой, разбавленной 1:100. Фильтрат и промывные воды сохраняют (основной раствор). Фильтр с осадком помещают в платиновый тигель, высушивают, озоляют и прокаливают при 1000 — 1100 °С. Затем тигель с осадком охлаждают
Осадок смачивают 2 — 3 каплями воды, добавляют 3 — 4 капли серной кислоты, 3 — 4 см3 фтористоводородной кислоты и осторожно выпаривают содержимое тигля до удаления паров серной кислоты. Остаток в тигле сплавляют с 2 — 3 г калия пиросернокислого, выщелачивают водой при нагревании и присоединяют к основному раствору
К полученному раствору приливают 5 см3 10 %-ного раствора хлористого аммония, 20 — 40 см3 50 %-ного раствора винной кислоты и добавляют раствор аммиака до рН 8 — 10 по универсальному индикатору, затем соляную кислоту до рН 2 — 3 по универсальному индикатору, разбавляют горячей водой до 350 — 400 см3, нагревают до 50 — 70 °С, приливают 1 %-ный спиртовой раствор диметилглиоксима в количестве, соответствующем 10 см3 на каждые 0,01 г никеля, после чего приливают раствор аммиака до рН 8 — 10 по универсальному индикатору.
Раствор с выпавшим осадком диметилглиоксимата никеля оставляют при 50 — 70 °С на 1 ч. Осадок отфильтровывают на фильтр «белая лента», промывают 5 — 6 раз теплой водой.
После этого осадок растворяют на фильтре 50 см3 горячей соляной кислоты, разбавленной 1:1. Фильтр промывают 5 — 7 раз горячей водой, собирая фильтрат и промывные воды в стакан, в котором проводилось осаждение. К раствору приливают 5 см3 50 %-ного раствора винной кислоты, раствор аммиака до рН 8 — 10 по универсальному индикатору, соляную кислоту до рН 2 — 3 по универсальному индикатору и разбавляют горячей водой до 350 — 400 см3. Затем раствор нагревают до 50 — 70 °С, приливают 10 — 15 см3 1 %-ного спиртового раствора диметилглиоксима, после чего приливают раствор аммиака до рН 8 — 10 по универсальному индикатору. Раствор с выпавшим осадком оставляют при 50 — 70 °С на 1 ч.
Осадок количественно переносят в стеклянный фильтрующий тигель № 4, предварительно высушенный до постоянной массы при 110 °С и взвешенный. Осадок промывают 7 — 8 раз теплой водой. Тигель с осадком высушивают до постоянной массы при 110 — 120 °С, охлаждают в эксикаторе и взвешивают.
3.4. Обработка результатов
3.4.1. Массовую долю никеля (X) в процентах вычисляют по формуле
где т1 — масса осадка диметилглиоксимата никеля в анализируемой пробе, г;
m2 — масса осадка диметилглиоксимата никеля в контрольном опыте, г;
т — масса навески чугуна, г;
0,2032 — коэффициент пересчета диметилглиоксимата никеля на никель.
Таблица 2
|
Абсолютные допускаемые расхождения, % |
|
|
От 0,1 до 0,2 |
0,02 |
|
Св. 0,2 » 0,5 |
0,03 |
|
» 0,5 » 1,0 |
0,05 |
|
» 1,0 » 2,0 |
0,06 |
|
» 2,0 » 4,0 |
0,08 |
|
» 4,0 » 8,0 |
0,12 |
|
» 8,0 » 15,0 |
0,16 |
|
» 15,0 » 25,0 |
0,20 |
3.3 — 3.4.2. (Измененная редакция, Изм. № 1).
7. ОТБОР И ХРАНЕНИЕ ПРОБ ВОДЫ
Отбор проб производится в соответствии с требованиями ГОСТ Р 51592-2000 «Вода. Общие требования к отбору проб».
7.1. Пробы воды отбирают в стеклянные или полиэтиленовые бутыли, предварительно ополоснутые отбираемой водой. Объём отобранной пробы должен быть не менее 150 см3.
7.2. Пробы анализируют в день отбора или консервируют добавлением 5 см3 концентрированной азотной кислоты на 1 дм3 пробы (нельзя консервировать при наличии цианидов). Если требуется отдельно определить никель в растворимой и нерастворимой формах, часть пробы фильтруют (до консервации), в ней определяют растворенную форму.
7.3. При отборе проб составляется сопроводительный документ по утвержденной форме, в котором указываются:
цель анализа, предполагаемые загрязнители;
место и время отбора;
номер пробы;
должность, фамилия отбирающего пробу, дата.